欢迎进入B体育官方网站!
咨询热线:025-69790896
新思路!中山大学发现“癌王”胰腺癌临床管理靶点和潜在药物
作者:小编 | 发布时间: 2024-06-28 | 次浏览
吉西他滨耐药是胰腺导管腺癌(PDAC)化疗效果的主要障碍。因此,需要新的策略来使癌细胞对吉西他滨敏感。

胰腺导管腺癌(PDAC)是最具侵袭性的癌症之一,其5年生存率为10%,近80%的患者表现为局部或远处转移的不可切除疾病。基于吉西他滨的联合化疗策略仍然是晚期PDAC的主要治疗方法。PDAC患者对吉西他滨治疗的初始敏感性很常见,但耐药性的快速发展严重限制了该治疗方案的疗效。因此,探索提高PDAC对吉西他滨敏感性的方法,并发现治疗PDAC的吉西他滨耐药性新靶点至关重要。
在本研究中,研究人员构建了吉西他滨耐药的PDAC细胞,并用RNA序列对其进行了分析。采用综合方法,涉及来自多个数据库的生物信息学分析,TGFB2被确定为吉西他滨耐药PDAC的关键基因,并且与吉西他滨治疗反应不佳显著相关。患者来源的异种移植物(PDX)模型进一步证实了吉西他滨诱导的耐药性期间TGFB2表达的逐渐上调。沉默TGFB2表达可以增强吉西他滨对PDAC的化疗敏感性。
机制上,TGFB2通过METTL14介导的m6A修饰在转录后稳定,可以促进脂质积累,而增强的甘油三酯积累通过脂质组学分析显示驱动吉西他滨耐药性。TGFB2通过PI3K-AKT信号转导上调脂肪生成调节剂甾醇调节元件结合因子1(SREBF1)及其下游脂肪生成酶。此外,SREBF1负责TGFB2介导的脂肪生成,以促进PDAC中的吉西他滨耐药性。重要的是,TGFB2抑制剂欧前胡素联合吉西他滨在吉西他滨耐药PDAC PDX模型中显示出协同作用。这项研究为通过靶向TGFB2和脂质代谢来减轻PDAC吉西他滨耐药性的途径提供了新的思路,并开发了欧前胡素作为临床转化中很有前景的化学增敏剂的潜力。
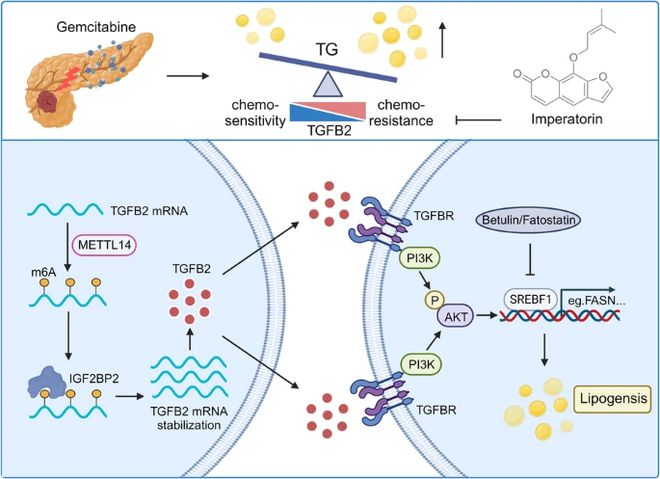
综上所述,研究首先证明N6-甲基腺苷修饰的TGFB2触发脂质代谢重编程以赋予胰腺导管腺癌吉西他滨耐药性。TGFB2抑制剂欧前胡素和吉西他滨的组合在吉西他滨耐药PDAC PDX模型中具有协同作用。研究结果表明,TGFB2和脂质代谢是PDAC临床管理的有希望的靶点,而欧前胡素是转化为临床试验的潜在药物。
转化医学网(是转化医学核心门户,旨在推动基础研究、临床诊疗和产业的发展,核心内容涵盖组学、检验、免疫、肿瘤、心血管、糖尿病等。如您有最新的研究内容发表,欢迎联系我们进行免费报道(公众号菜单栏-在线客服联系),我们的理念:内容创造价值,转化铸就未来!
转化医学网()发布的文章旨在介绍前沿医学研究进展,不能作为治疗方案使用;如需获得健康指导,请至正规医院就诊。

特别声明:以上内容(如有图片或视频亦包括在内)为自媒体平台“网易号”用户上传并发布,本平台仅提供信息存储服务。
vivo被印度塔塔收购,为何国家不像挺华为、TikTok一样挺vivo
近900万,胖东来“最贵的擀面皮”!顾客排长龙办退款,工作人员:宁可赔钱也不能给我们品牌抹黑【附超市行业现状分析】
与中坚力量共成长,2024建信信托艺术大奖评委会特别奖获奖艺术家凌海鹏
红魔首款游戏本搭载 16 英寸 240Hz 高刷屏,100% DCI-P3 色域
国内已有51所职业本科院校,有学校录取分数堪比211,能上211你还会选职业本科吗?